イレッサ事件の概要
背景
医薬品の副作用死
医薬品には副作用がない方が望ましいが、効果のあれば何らかの副作用も生じる。 劇的な効果のあって、かつ、副作用がない医薬品は存在しない。 市販薬でも副作用による死亡例はある。 もちろん、市販薬の安全性は重要であるが、100%完璧なものは存在しない。
抗がん剤の副作用死
“薬害”イレッサの背景に記載している通り、がんの根治が難しい場合は、長期延命(実質的完治含む)や疼痛緩和が目的となる。 そして、効き目や副作用には個人差があり、ある人には有効な治療法が別の人には効かない。 また、抗がん剤は、長く使っていると腫瘍が耐性を持つため、耐性後は別の治療法に切り替える必要がある。 そのため、がんの治療法は1種類では足りず、何種類もの治療法が必要になる。 しかし、がんの種類によっては、十分な種類の治療法が確立されていないことも珍しくはない。
「この薬を飲めば立ち所にがんが治る」という薬はないし、現代医学では作れない。 だから、強い副作用のある薬であっても、それ以上の効果があれば使わざるを得ない。 死亡する恐れのある副作用があっても、副作用死を上回る命を救えるなら、他に選択肢がなければ、使わざるを得ない。 当然、副作用死が全くなく、かつ、多くの命を救える薬があれば、それに越したことはない。 しかし、現状ではそんなものはないのだから、死亡する恐れのある副作用のある薬も使わざるを得ない。
目の前に放置すれば確実に24時間以内に死亡する患者が居たとしよう。 そして、治療すれば99%の確率で治癒するが、1%の確率で即死するとする。 この場合は治療を行うべきか否か。 患者の損得を考えれば治療すべきであることは言うまでもなかろう。 しかし、1%の確率で即死することの責任を問われたら治療はできない。 しかも、放置したことに責任を問われないなら、医師個人にとっては放置がベストの選択になってしまう。 果たして、救える命を見殺しにすることが正しい選択だろうか。 リスクよりもベネフィットが上回る場合にでも「副作用で死ぬなんてけしからん」と主張するなら、まさにこれと同じ問題である。
もちろん、死のリスクは可能な限り低減した方が望ましい。 しかし、現代医学の最高峰をもってしても死のリスクをゼロにすることはできない。 それでも回避できない死は医療関係者の責任なのか。 強いて言うなら、そうした運命を強いる神の責任であろう。
日本では、ドラッグ・ラグや未承認薬の問題があり、欧米で使える薬が日本で使えないことも多い。 とくに、特許が切れている医薬品は開発コストの回収が難しいので製薬会社は申請したがらない。 確立した治療法の新規承認は絶望的な状況であり、新規医薬品の開発を促進するしかない状況である。
そうした中で、医薬品の審査が迅速化された。 尚、迅速化されたのは提出された申請書類の審査である。 効果実証のための治験等の手続きが免除されたわけではない。 抗がん剤の承認基準に記載している通り、それ以前の抗がん剤もイレッサも国際的なRECISTガイドラインに基づいて効果判定されている。
事件
イレッサの副作用
イレッサ最高裁判決文によれば、承認時のイレッサの間質性肺炎による副作用死率は次のとおりである。
| 試験 | 症例数 | 間質性肺炎発症数 | 副作用の疑いのある死亡数 | 副作用死率 | 備考 |
|---|---|---|---|---|---|
| 国内臨床試験 | 133 | 3 | 0 | 0.00% | |
| 国外臨床試験 | 1000以上 | 5 | 4 | 0.4%以下 | イレッサ投与と死亡との因果関係は可能性ないし疑いがある程度 |
| 拡大供給プログラム | 約15000 | 15 | 9 | 約0.06% | イレッサ投与と死亡との因果関係は否定はしきれないものの肯定することまではできない |
抗がん剤の副作用死は仕方ない?に記載している通り、第5回 市民公開講演会「がんについて」抗がん剤の有効性と危険性 - 国立がん研究センターによれば、塩酸イリノテカン(CPT-11)の副作用死率は臨床試験中で4.4%であり、市販後は0.77%である。 以上の通り、承認時に分かっていたイレッサの副作用率は、他の抗がん剤に比べて極めて良好だった。
そして、承認当時、イレッサと間質性肺炎の因果関係は明確ではなかった。 というのも、がんの進行によっても間質性肺炎が発生するからである。 後から判明したことであるが、イレッサによって間質性肺炎になるのではなく、既に密かに発生していた間質性肺炎がイレッサによって急激に進行するのである。 だから、状態の悪い患者にイレッサを投与して間質性肺炎を発症しても、それががんの進行によるものか、あるいは、イレッサによるものかは見分けがつきにくい。 最高裁判決文p.6でも、「早期に発症し急速に進行する間質性肺炎が副作用として存在することをうかがわせるものではなかった」とされている。 イレッサと間質性肺炎の因果関係が明確になったのは、市販後に通常ではあり得ないほどの間質性肺炎の症例が相次いだためである。
イレッサの添付文書
イレッサ最高裁判決文によれば、承認当時、「患者の体質や発現時の状態等によっては,死亡又は日常生活に支障をきたす程度の永続的な機能不全に陥るおそれのあるもの」を記載する欄である「重大な副作用」欄に間質性肺炎が記載されていた。 すなわち、当初から、添付文書にて間質性肺炎による「死亡又は日常生活に支障をきたす程度の永続的な機能不全に陥るおそれ」は警告されていた。
尚、間質性肺炎は、重度の下痢、中毒性表皮壊死融解症,多形紅斑、肝機能障害の後に記載されていたが、最高裁判決文p.5-6によれば、いずれも、「患者の体質や発現時の状態等によっては,死亡又は日常生活に支障をきたす程度の永続的な機能不全に陥るおそれのあるもの」であった。
厚生労働省の対応
イレッサ薬害を沈静化した国の迅速な緊急安全性情報に記載している通り、ゲフィチニブ服用後の急性肺障害・間質性肺炎等に係る副作用報告の報告件数等について - 厚生労働省、ゲフィチニブによる急性肺障害、間質性肺炎についての「緊急安全性情報」の発出について - 厚生労働省によれば、製薬会社から11例の死亡報告、および、医療機関から2例の死亡報告があった時点で、緊急安全性情報にて注意喚起するよう製薬会社に指示している。 抗がん剤での副作用死が珍しくないことを考えると、この厚生労働省の対応は非常に迅速であろう。
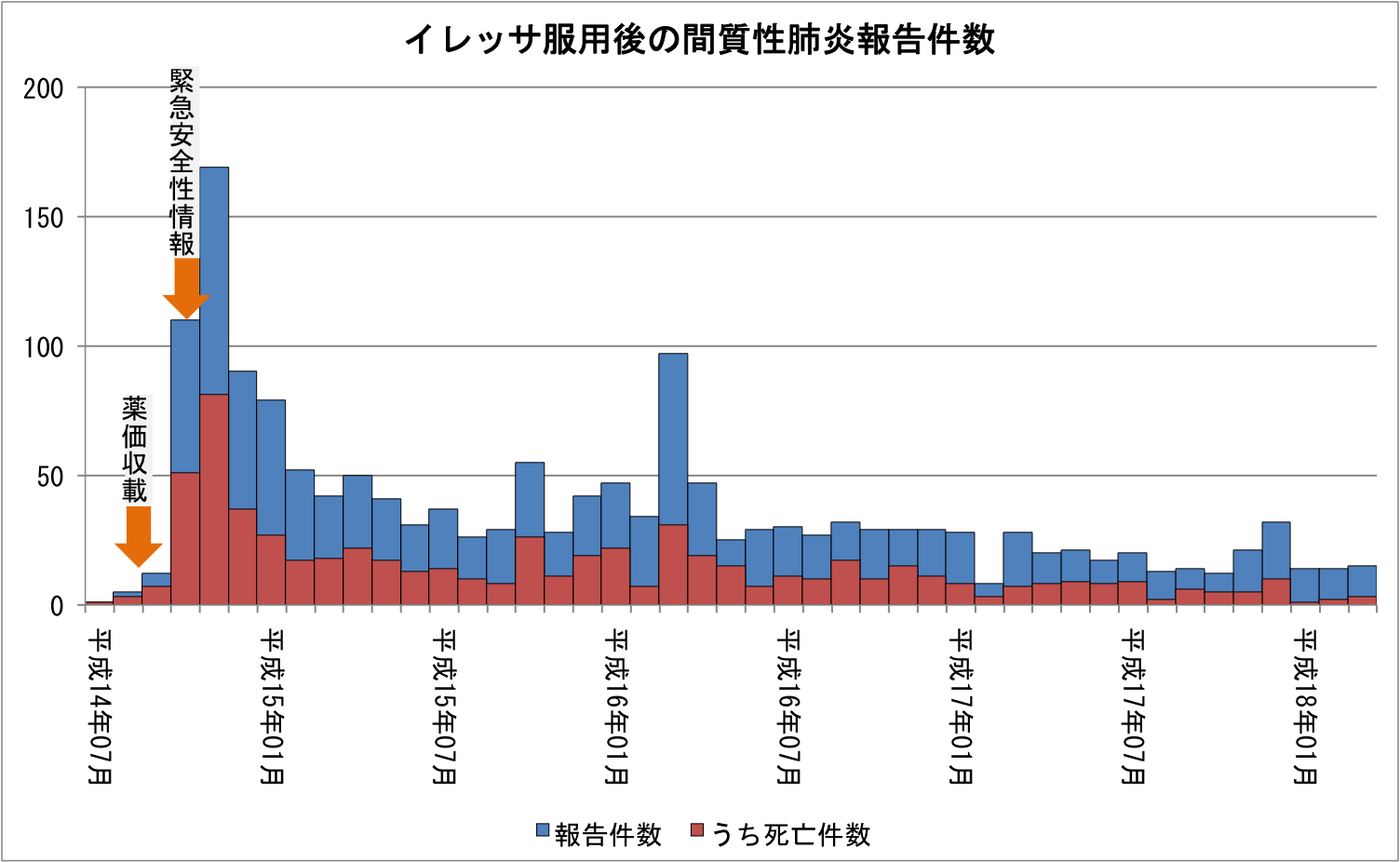
ゲフィチニブ服用後の急性肺障害・間質性肺炎等に係る副作用報告の報告件数等について - 厚生労働省
医師の責任
医師の処方が必要な医療用医薬品の添付文書の対象は患者ではなく医師であることは、イレッサ大阪高裁判決でもイレッサ東京高裁判決でも認められている。
イレッサ訴訟原告が医師を訴えない謎に記載している通り、平成4(オ)251 損害賠償請求事件 平成8年01月23日 最高裁判所第三小法廷では、「医療水準は、医師の注意義務の基準(規範)となるものであるから、平均的医師が現に行っている医療慣行とは必ずしも一致するものではなく、医師が医療慣行に従った医療行為を行ったからといって、医療水準に従った注意義務を尽くしたと直ちにいうことはできない。 」「医師が医薬品を使用するに当たって右文章に記載された使用上の注意事項に従わず、それによって医療事故が発生した場合には、これに従わなかったことにつき特段の合理的理由がない限り、当該医師の過失が推定されるものというべきである。」と判示されている。 また、平成12(受)1556 損害賠償請求事件 平成14年11月08日 最高裁判所第二小法廷では、「必要に応じて文献を参照するなど,当該医師の置かれた状況の下で可能な限りの最新情報を収集する義務があるというべきである。」と判示されている。
承認当時、添付文書よりも有力な医学情報は皆無であり、添付文書における間質性肺炎の警告に対して「これに従わなかったことにつき特段の合理的理由がない」ことは明らかである。 よって、添付文書に従わなかったことによる副作用死や、患者へのインフォームドコンセントは全て医師の責任である。
掌を返したマスコミ
承認前は、夢の新薬と持て囃したマスコミが、事件後は、一転、イレッサを悪魔の薬として批判した。
薬害ゴロの介入
悪魔の薬“薬害”イレッサ訴訟に記載している通り、浜六郎氏の率いる薬害オンブズパーソンなる薬害ゴロがやり場のない感情を抱えた原告たちに訴訟を起こすよう唆したのである。
裁判
偏向報道
社説イレッサ…と言う名のプロパガンダ(情報操作)に記載している通り、マスコミ各社は、事実関係や判決文を自ら調べることなく、原告の主張をそのまま記事に掲載した。
原告の主張
イレッサ弁護団の詭弁に記載している通り、原告は、医師の責任を転嫁したり、国の主張を歪曲したりしている。 また、原告は、緊急安全性情報や添付文書の改訂などによって被害が激減している事実をもって、添付文書の記載に不備があったと主張する。 しかし、その事実が示す可能性は、次の2通りある。
- 当初の対応は適切だったにも関わらず予想外の副作用被害が多発し、その後の処置で「被害が激減」した。
- 当初の対応が不適切なために予見可能な副作用被害が多発し、その後の処置で「被害が激減」した。
この事実からは、副作用被害が多発したこととその後の処置が適切だったことは確実に言えるが、副作用被害が多発することを予見可能であったかどうかまでは分からない。 よって、この事実は、承認当初の添付文書の記載に不備の根拠とならない。 結果的に副作用被害が多発した等によって添付文書の記載に不備があったと主張することは、「後知恵に基づく批判」「後方視的な批判」以外の何物でもない。 「後知恵に基づく批判」「後方視的な批判」を正当化したいなら、タイムマシンを開発すべきだろう。
和解勧告
あたかも裁判所が自発的に和解勧告を出したかのように報じられ、原告は和解勧告を受け入れない国や製薬会社を非難した。 しかし、薬害イレッサ訴訟和解勧告の真相に記載している通り、原告側から和解勧告を求める上申書を提出したから和解勧告が出たのであり、裁判所が自発的に和解勧告を行ったわけではない。 ようするに、裁判では勝てそうもないから、原告は和解勧告上申という変則的な手口を使ったに過ぎない。
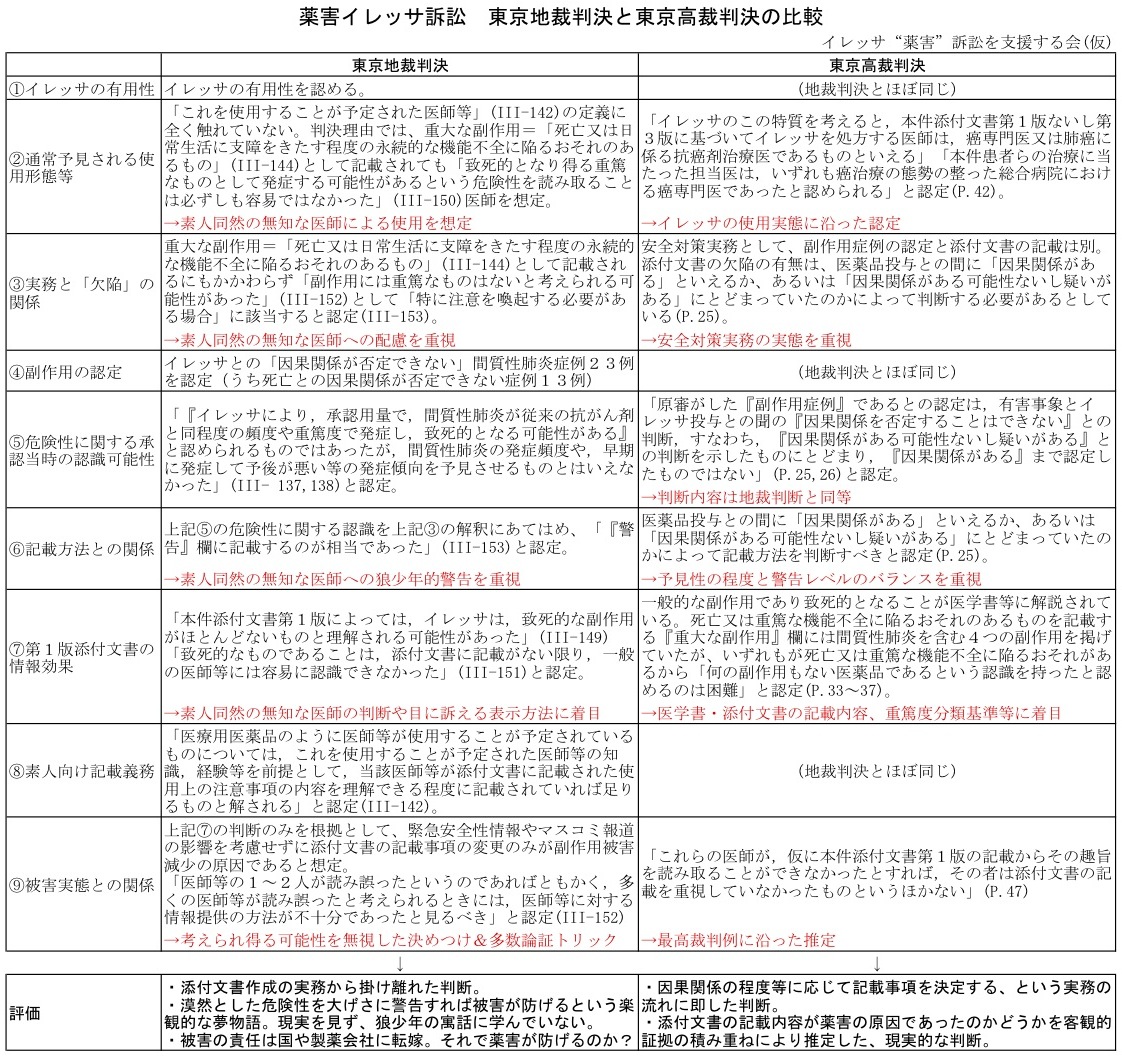
地裁判決
イレッサ訴訟東京地裁判決、イレッサ訴訟大阪地裁判決とも、認定事実に対して論理的に辻褄の合わない原告有利の判決を下している。
東京地裁判決、大阪地裁判決とも、イレッサ承認当時に、間質性肺炎の副作用が死に至る副作用である“可能性”を認識できたとしている。 その一方で、発生頻度(何人中何人が発症するか)や発症傾向(予後がどれだけ悪いか)を正確に把握することは困難だったとも認定している。 つまり、どちらの判決においても、承認当時、イレッサの間質性肺炎は、死ぬことが“確実”な副作用だとは分からなかったが、死ぬことも“あるかもしれない”副作用だと分かっていたと認定した。
イレッサ東京高裁判決では「重大な副作用」欄の記載すべき事項は「死亡又は日常生活に支障をきたす程度の永続的な機能不全に陥るおそれのあるもの」であると認定した。 にも関わらず、東京地裁判決は「致死性のあるもののみが記載されることとはされていないこと」として、「致死的となり得る重篤なものとして発症する可能性があるという危険性を読み取ることは必ずしも容易ではなかった」としている。 しかし、これは、単なる言葉遊びに過ぎない。 「永続的な機能不全」は後遺障害が残ることを意味し、それが「日常生活に支障をきたす程度」であれば、かなり重度の後遺障害である。 患者の立場に立てば、死亡も重度後遺障害も甲乙つけ難いほどの重大な不利益であって、どちらも、絶対に避けるべき副作用であろう。 だから、重度後遺障害のおそれのある副作用であれば、当然、死亡のおそれのある副作用と同程度に警戒する必要がある。 よって、「重大な副作用」欄に記載すれば、死亡のおそれのある副作用と同程度に警戒すべき副作用だと警告したことになるはずである。
- イレッサの間質性肺炎は、死ぬことも“あるかもしれない”副作用だとは分かっていた。
- 「重大な副作用」欄の記載事項は、死亡を含めて重度後遺障害のおそれのある以上の副作用であった。
これら前提事実によれば、「重大な副作用」欄に記載すれば、少なくとも重度後遺障害のおそれのある副作用であることは警告できている。 そして、それならば、死亡のおそれのある副作用と同程度に警戒すべきだったことも十分に示せている。 承認当時、イレッサの間質性肺炎は死亡のおそれのある副作用だとの認識だったので、死亡のおそれのある副作用と同程度に警戒すべき副作用だと警告できれば、国の認識とほぼ同じ内容の警告を発したことになろう。 よって、地裁判決の前提事実からは、間質性肺炎を「重大な副作用」欄に記載したイレッサの第1版添付文書の危険性の警告が不十分とは言えない。 もちろん、道義的には、第1版添付文書の書き方よりも強い警告を発しても間違いではなかったとは言える。 しかし、地裁判決の前提事実では、法的責任を問うほどの過失があったとする根拠が示されていない。
大阪地裁判決では、間質性肺炎が下痢、皮膚障害、肝機能障害の後に書かれていたために「重要とは考えられないものと解釈されるおそれのある記載であった」としている。 しかし、イレッサの承認当時、その3つの副作用は、いずれも、死亡のおそれのある副作用であった。 それは、大阪地裁が承認当時にその3つの副作用の死亡例が確認されているとしていることからも明らかである。 死亡のおそれのある副作用より後に書かれていて、どうして、間質性肺炎は死亡のおそれがないと誤解される余地があるのか。
- 下痢が多大な副作用死被害をもたらしたかもしれない
- 皮膚障害が多大な副作用死被害をもたらしたかもしれない
- 肝機能障害が多大な副作用死被害をもたらしたかもしれない
イレッサ承認当時には、いずれも、間質性肺炎と同程度には起きる可能性のある“薬害”候補だった。 蓋を開けてみれば、間質性肺炎だけが多大な副作用死被害をもたらした。 しかし、それは、実際に承認して沢山の使用実績を積み重ね後に分かった結果論である。 大阪、東京の両地裁のどちらにおいても、イレッサの承認当時に、間質性肺炎が他の3つの副作用よりも特別危険だと判断できたとする医学的根拠は示されていない。 それなのに、どうして、承認当時に、間質性肺炎を1番目に書くべきだったと言えるのか。 どうして、承認当時に、間質性肺炎だけを「警告」欄に書くべきだったと言えるのか。 間質性肺炎が他の3つの副作用よりも特別危険だと分かったのは、後から分かったことである。 タイムマシンでもなければ、後から分かったことを、承認当時の添付文書に書くことはできない。 このような無茶を言われると、死亡の恐れのある副作用は次のように書かざるを得ない。

これが正しい対応なのか、よく考えてもらいたい。 対策としてやるべきことは、人為的な狼少年効果を発生させることではなく、医者に「重大な副作用」欄の意味を正しく認識させることだろう。
学会および患者団体の意見
地裁判決に対して、学会やがん患者団体から薬事行政が歪められる懸念の意見表明が相次いだ。 それに対して、原告は、国が圧力をかけたからだと主張する。 しかし、いわゆる『下書き』提供問題調査報告書声明に対する声明に記載している通り、各学会は独自の意見を表明したにすぎない。 そもそも、患者団体にはそのような圧力は通用しない。 患者団体はイレッサ“薬害”の見解を述べよ!に記載している通り、原告は、がん患者団体から総スカンを喰らっている。
高裁判決
イレッサ大阪高裁判決でも、イレッサ東京高裁判決でも、次のように認められた。
- イレッサ の承認は妥当
- 医療用医薬品の添付文書は医師に分かるように書けば良い
- 「重大な副作用」欄に記載すべきものは死亡又は重篤な機能不全に陥るおそれがあるもの
- 記載された4つの副作用には、いずれも、死亡のおそれがあった
- 添付文書第1版の記載から間質性肺炎の致死性の可能性を読み取ることが可能
最高裁判決
最高裁判決は高裁判決を追認したに過ぎない。
メニュー
経緯
判決内容
注意事項
医療問題
全般
イレッサ
偏向報道
- 社説イレッサ…と言う名のプロパガンダ(情報操作)
- イレッサ声明文案下書き問題(世論誘導)
- 予防原則の常識を根底から覆すイレッサ逆転無罪判決?
- イレッサ判決で原告が逆転敗訴・日本の「予防原則」が死んだ日?
訴訟
解説
- イレッサ指示・警告上の欠陥を常識で考える
- 予防原則に沿ったイレッサ高裁判決
- イレッサ大阪高裁判決速報
- イレッサ東京訴訟上告理由不備
- イレッサ訴訟トンデモ判決の原因分析
- イレッサ東京訴訟地裁判決と高裁判決の比較
- イレッサ東京高裁判決速報
- J&T治験塾への反論
- イレッサ訴訟地裁判決の問題点(MRIC)
- 製造物責任法とは?
原告の姿勢等
- イレッサ薬害訴訟の問題点
- 糾弾されるべきイレッサ訴訟原告
- イレッサ弁護団の詭弁
- イレッサ訴訟原告が医師を訴えない謎
- 99%の遺族がイレッサ訴訟原告に居ない事実
- 薬害イレッサ訴訟和解勧告の真相
- イレッサ原告また厚労相協議申入なる奇策
- 裁判所勧告を受けた国のコメントに関するQ&A
- “薬害”イレッサ訴訟・控訴抗議に対する抗議声明
- “薬害”イレッサ訴訟・原告控訴に対する抗議声明
- いわゆる『下書き』提供問題調査報告書声明に対する声明
- 7月27日「こんな癒着は許さない!薬害イレッサ脳内集会」を開催します!
- 薬害イレッサ訴訟東京高裁判決についての原告団・弁護団声明についての声明
- イレッサ原告の十八番=結果後付論法
- イレッサ大阪高裁判決院内報告集会における詭弁
- イレッサ薬害死亡者数の水増し(本当は70人強)
- イレッサ弁護団は馬鹿?
- 患者の治療の道を閉ざす原告の犬
関係団体等
- イレッサ薬害を沈静化した国の迅速な緊急安全性情報
- 患者団体はイレッサ“薬害”の見解を述べよ!
- “薬害”イレッサ訴訟で国と製薬会社の控訴は当然
- 国と製薬会社はイレッサ訴訟の求償権を行使して医師を訴えよ!